Aula Prática: Será que o ar ocupa espaço?
Autor: Edilaine Viana - 16/09/2023 - 20:05 - 3.1K
O Ar
AULA PRÁTICA: SERÁ QUE O AR OCUPA ESPAÇO?
HABILIDADE:
EF07CI12: Demonstrar que o ar é uma mistura de gases, identificando sua composição, e discutir fenômenos naturais ou antrópicos que podem alterar essa composição.
A composição da atmosfera terrestre inclui vários gases dispersos, tais como hidrogênio, nitrogênio, gás carbônico e oxigênio. Dentre esses gases, o oxigênio corresponde a aproximadamente 21% do total. O oxigênio desempenha um papel essencial para os seres vivos aeróbicos, ou seja, aqueles que necessitam desse gás para a respiração.
O oxigênio é uma molécula composta por dois átomos do elemento oxigênio, e é um dos componentes responsáveis pelo fenômeno do fogo.
Embora tudo que exista e ocupe um lugar no espaço seja feito de matéria, surge a pergunta: o oxigênio é feito de matéria? Além disso, será que esse gás ocupa um lugar no espaço?
OBJETIVO: Comprovar que o ar existe e ocupa um lugar no espaço como qualquer matéria.
MATERIAIS:
Copo;
Vela Placa de Petri ou prato;
Água
PROCEDIMENTOS:
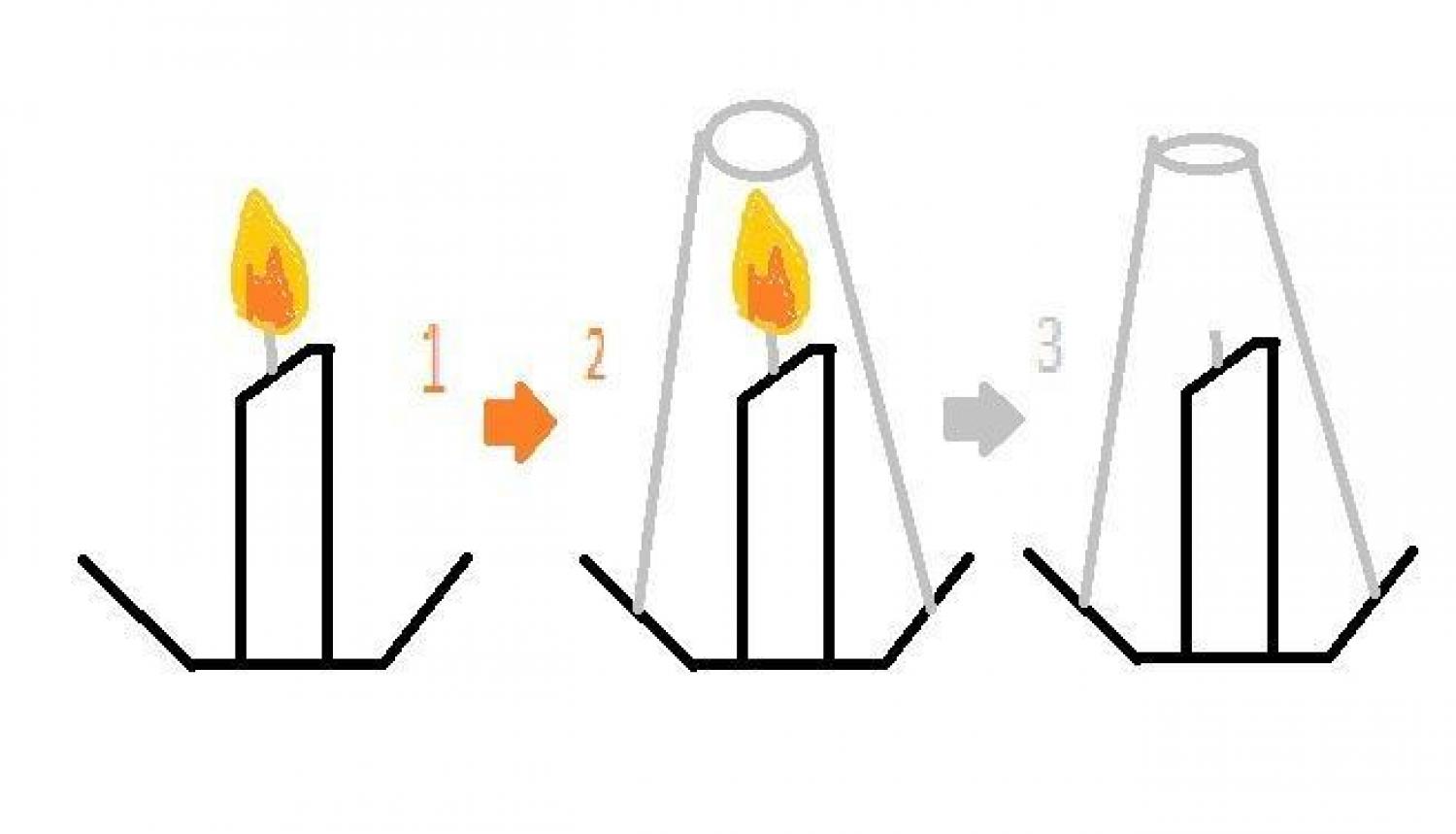
1º Colocar a vela acesa colada na Placa de Petri ou prato;
2º Colocar um pouco de água na Placa de Petri ou prato;
3º Colocar um copo grande sobre a vela cobrindo-a;
DISCUSSÃO:
1. O que aconteceu quando colocamos o copo sobre a vela?
2. Por que isto aconteceu?
3. Faça um desenho deste experimento seguindo as três etapas.
a) Colocar a vela acesa na Plata de Petri ou Prato
b) colocar água na placa de Petri ou Prato
c) Cobrir e vela
EXPLICAÇÃO:
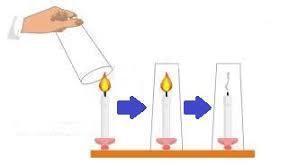
Para que ocorra a combustão, é necessário a presença de oxigênio gasoso (O2). Quando você coloca um copo sobre uma vela acesa, o ar dentro do copo fica confinado, o que significa que o oxigênio disponível para a combustão é limitado. À medida que a vela consome o oxigênio dentro do copo, a quantidade disponível diminui gradualmente.
Consequentemente, a vela consome todo o oxigênio disponível dentro do copo e, eventualmente, não há oxigênio suficiente para sustentar a combustão. Como resultado, a chama se apaga devido à falta de oxigênio necessário para a reação de combustão.
BAIXAR AULA PRÁTICA: